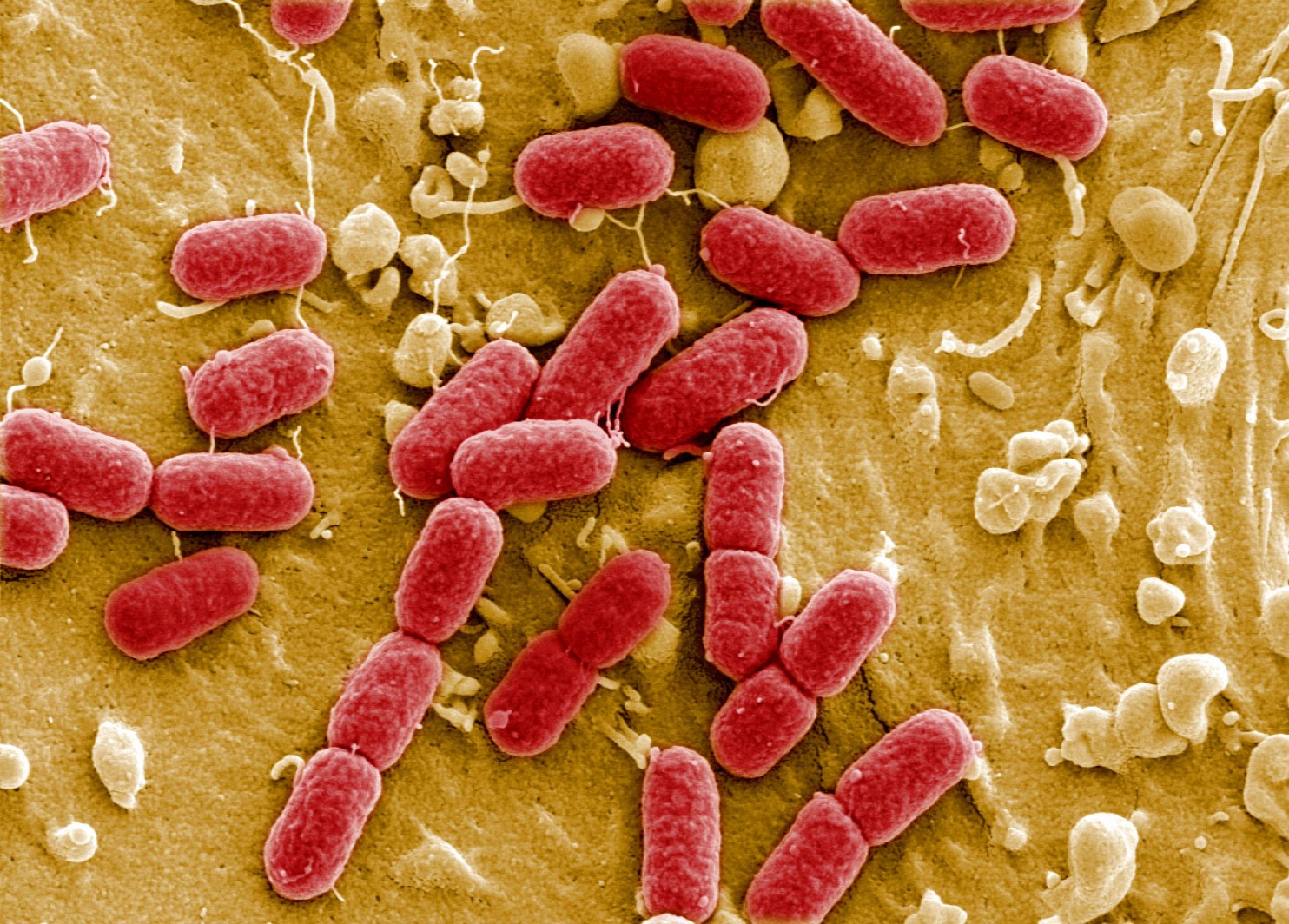
Бактерии печально известны своей способностью к развитию устойчивости к самым мощным антибиотикам. Являясь преимуществом для бактерий, это их умение приводит к появлению миллионов плохо поддающихся лечению инфекций по всему миру, равно как и опасений, что однажды бактерии могут стать непобедимыми в принципе. Однако эволюционное преимущество этих микроорганизмов может также обернуться их ахиллесовой пятой, как следует из доклада ученых, сделанном на прошлой неделе и опубликованном в Nature Chemical Biology.
…эволюционное преимущество этих микроорганизмов может также обернуться их ахиллесовой пятой, как следует из доклада ученых…
Экспериментируя с условиями эволюции бактерий, исследователям удалось обмануть устойчивые к лекарствам штаммы кишечной палочки и те лишились своей защиты. После последующего применения лекарственного препарата, к которому у бактерий прежде имелась устойчивость, кишечные палочки погибли.
И хотя исследование проводилось в лабораторных условиях, авторы, во главе с исследователями из Гарвардского университета (Harvard University), надеются, что примененная двухходовка может быть полезной в преодолении лекарственной устойчивости микробов и восстановлению эффективности большого количества некогда действенных антибиотиков. Подобный двухступенчатый подход может “добавить ценное оружие в наш противомикробный арсенал”, – заключают они.
Попытаться обмануть бактерии ученые решили исходя из факта, что многие типы резистентности микробов основаны на извлечении выгоды из недостатков антибиотиков. Иными словами, не все типы лекарственной устойчивости одинаково надежны, они зависят от типа антибиотика, устойчивость к которому развили бактерии.
Работа некоторых антибиотиков, таких как Ципрофлоксацин и других фторхинолонов, подобна гаечному ключу, брошенному в момент и место деления бактериальных клеток, в то время как других, таких как пенициллин и ему подобных, подобна кислоте, растворяющей стенки бактериальных клеток (лизис), превращающей их в дырявое месиво. Третьи же, такие как тетрациклины и аминогликозиды (например, Стрептомицин), портят синтез белка в бактерии, привнося неразбериху в важные биологические процессы микробов.
…некоторые микробы маскируют компонент стенок своих клеток, который должен блокировать лекарственный препарат. Другие бактерии заимели ферменты, чтобы разлагать антибиотики или даже обзавелись специальными насосами, откачивающими медикаменты из бактериальной клетки…
Бактерии развили в себе “умные” защитные механизмы против большинства антибиотиков. Некоторые бактерии использовали эволюционные мутации для маскировки основной цели удара антибиотика.
Например, некоторые микробы, имеющие резистентность к пенициллину, маскируют компонент стенок своих клеток, который должен блокировать лекарственный препарат. Другие бактерии заимели ферменты, чтобы разлагать антибиотики или даже обзавелись специальными насосами (efflux pump), откачивающими медикаменты из бактериальной клетки пока те не навредили ей.
Иногда эти новые стратегии сопротивления возникают на основе мутаций, возникающих в бактериальной популяции, получившей нелетальную дозу препарата. Однако, значительная доля сопротивляемости связана с передачей уже развитых узкоспециализированных генов, которыми бактерии могут обмениваться друг с другом тем или иным способом (при помощи передачи колец ДНК, называемых плазмидами или благодаря мобильным участкам ДНК — транспозонам — также известным как «прыгающие гены»).
Уязвимость защиты бактерий от антибиотиков
Зная в деталях особенности устойчивости популяции бактерий к определенному антибиотику можно пробовать обнаружить слабость в системе защиты, утверждают авторы доклада. Например, для генерации некоторых ферментов, растворяющих лекарства, может требоваться много энергии. И если бактерия в значительной степени нуждается в ресурсах и при этом не находится под действием антибиотика, она сама может уничтожать плазмиды, несущие “чертежи” фермента. Кроме того, существуют гены устойчивости, делающие бактерию невосприимчивой к одному препарату, но неизбежно приводящие к увеличению восприимчивости к другому — сценарий, который был впервые описан в 1952 и получил название “побочной чувствительности” (collateral sensitivity).
С тех пор ученые выявили множество случаев бактерий с побочной чувствительностью, приобретенной в результате обычной эволюционной мутации. Но они нашли только несколько экземпляров бактерий с побочной чувствительностью, резистентность которых передавалась описанными ранее развитыми специализированными противолекарственными генами. Авторы задались целью найти больше таких штаммов бактерий и использовать их для обращения эволюции вспять.
Ученые сконцентрировали свое внимание на бактериях E. coli (Escherichia coli, кишечной палочки), которые стали невосприимчивыми к тетрациклину благодаря специальным откачивающим насосам, генетический код которых содержится в транспозонах (прыгающих генах) ДНК указанных бактерий.
Проблема резистентности к тетрациклину широко распространена в медицинской и сельскохозяйственной сферах, что делает его бесполезным во многих случаях.
В значительной степени эта невосприимчивость к тетрациклину предопределена именно передачей резистентности прыгающими генами, транспозонами.
Ученым пришлось провести значительное количество тестов, выбирая из 19769 соединений химической библиотеки те, которые бы уничтожили тетрациклин-устойчивые штаммы кишечной палочки, но оставили бы штаммы обычной кишечной палочки относительно невредимыми. Они нашли два таких вещества: Дисульфирам (Disulfiram, Antabuse) для лечения алкоголизма — препарат, одобренный FDA (управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США) и Бета-Туяплицин (β-Thujaplicin), как известно, обладающий противогрибковым и антибактериальным действием.
Поскольку тетрациклиновая резистентность сделала бактерии чувствительными к Бета-Туяплицину, общее направление противодействия популяции действию медикамента оказалось таковым, что в результате разрушило их систему защиты от тетрациклина…
Действие Бета-Туяплицина оказалось более избирательным, поэтому в дальнейшем исследователи использовали только его. Далее, в течение недели они вырастили 8 одинаковых популяций кишечной палочки, воздействуя на каждую нелетальной дозой Бета-Туяплицина.
Поскольку тетрациклиновая резистентность сделала бактерии чувствительными к Бета-Туяплицину, общее направление противодействия популяции действию медикамента оказалось таковым, что в результате разрушило их систему защиты от тетрациклина, основанной на переносе генетического кода транспозонами.
В результате чего 7 из 8 популяций окончательно потеряли свою тетрациклиновую резистентность благодаря непроизвольному уничтожению “чертежей насосов” в транспозонах в попытке противостоять новому лекарству. После чего бактерии были легко уничтожены тетрациклином.
Тем не менее, в одной из семи популяций, в которой бактерии не потеряли резистентность к тетрациклину, в результате оказались бактерии, невосприимчивые к обоим препаратам.
И хотя подобный результат, казалось бы, выхолащивает саму идею эволюционного подхода к уничтожению бактерий, ученые замечают, что он значительно менее вероятен, чем желаемый. Среди недостатков этого способа лечения можно также отметить предположительно более длительные сроки лечения, что делает его невозможным для лечения пациентов, уже находящихся в тяжелом состоянии. “Несмотря на описанные трудности, мы надеемся, что результаты этого исследования вдохновят будущих исследователей на создание терапевтических парадигм, которые смогут повернуть вспять эволюцию антибиотикорезистентности”.
Источник:
Survival of the smartest: Superbugs defeated with evolutionary trick
http://arstechnica.com/science/2016/09/scientists-turn-superbugs-into-sitting-ducks-with-evolutionary-hoodwink/#p3